实验动物编号标记方法
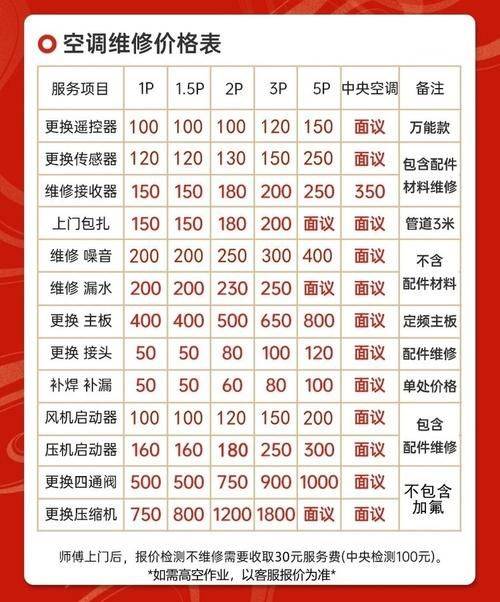
动物在实验前常常需要作适当的分组,那么就要将其标记使各组加以区别。标记的方法很多,良好的标记方法应满足标号清晰、耐久、简便、适用的要求。 常用的标记法有染色、耳缘剪孔、烙印、号牌等方法。 (一)颜料涂染 这种标记方法在实验室最常使用,也很方便。使用的颜料一般有3-5%苦味酸溶(黄),2%硝酸银(咖啡色)溶液和0.5%中性品红(红色)等。标记时用毛笔或棉签蘸取上述溶液,在动物体的不同部位涂上斑点,以示不同号码。编号的原则是:先左后右,从上到下。一般把涂在左前腿上的计为1号,左侧腹部计为2号,左后腿为3号,头顶部计为4号,腰背部为5号,尾基部为6号,右前腿为7号,右侧腰部为8号,右后腿计为9号。若动物编号超过10或更大数字时,可使用上述两种不同颜色的溶液,即把一种颜色作为个倍数,另一种颜色作为十位数,这种交互使用可编到99号,假使把红的记为十位数,黄色记为个位数,那么右后腿黄斑,头顶红斑,则表示是49号鼠(图......阅读全文
实验动物的麻醉方法1
麻醉(anesthesia)的基本任务是消除实验过程中所至的疼痛和不适感觉,保障实验动物的安全,使动物在实验中服从操作,确保实验顺利进行。一、常用的麻醉药(一)常用局部麻醉剂:普鲁卡因,此药毒性小,见效快,常用于局部浸润麻醉,用时配成0.5%~1%;利多卡因,此药见效快,组织穿透性好,常用1%~2%
实验动物标本的采集方法
实验概要本文介绍了实验动物标本(脑脊液、骨髓、消化液、腹水、胸水、尿液等)的采集方法。实验步骤1. 脑脊液的采集 1) 脊髓穿刺法狗、兔脑脊液的采集通常采取脊髓穿刺法。穿刺部位在两髂连线中点稍下方第七腰椎间隙。动物轻度麻醉后,侧卧位固定,使头部及尾部向腰部尽量弯曲,剪去第七腰椎周围的被毛。消毒
肠溶剂动物药理实验的方法
1、选择那种动物比较好?用Beagle犬比较多。2、怎么实验动物给药?方法是使狗的嘴张开并固定,头稍抬起,用镊子把胶囊或是片子放在舌后部,倒少量的水,如果是胶囊水不能太多否则胶囊会漂起来,然后动作快点放开固定,Beagle犬很温顺一般不会有什么问题 。口服制剂用兔子的也比较多,但一般需要将药物粉碎后
实验动物体液采集方法
一、血液的采集常用的采血方法有割(剪)尾采血、眼眶静脉丛采血、断头采血、心脏采血、颈静脉(动脉)采血、股动脉(静脉)采血、耳静脉采血、前肢头静脉才学、后肢小静脉采血等。二、尿液的采集实验动物的尿液常用代谢笼采集,也可通过其他装置来采集。(一)用代谢笼采集尿液代谢笼用于收集实验动物自然排出的尿液,是一
实验动物给药途径和方法
(六)淋巴囊注射蛙类常采用此法,因其皮下有数个淋巴囊,注入药物甚易吸收。腹部淋巴囊和头背淋巴囊常作为蛙类给药途径。一般多选用腹部淋巴囊给药。注射时将针头从蛙大腿上端刺入,经大腿肌层入腹壁肌层,再进入腹壁皮下,即进入淋巴囊,然后注入药液。有时也可采用胸淋巴囊给药。方法是将针头刺入口腔,使穿过下颌肌层入
实验动物给药途径和方法
在动物实验中,为了观察药物对机能功能、代谢及形态引起的变化,常需将药物注入动物体内。给药的途径和方法是多种多样的,可根据实验目的、实验动物种类和药物剂型等情况确定。 (一)皮下注射 注射时以左手拇指和食指提起皮肤,将连有5(1/2)号针头的注射器刺入皮下。皮下注射部位一般狗、猫多在大腿外侧,豚
实验动物体液采集方法
实验动物体液采集方法一、 血液的采集常用的采血方法有割(剪)尾采血、眼眶静脉丛采血、断头采血、心脏采血、颈静脉(动脉)采血、股动脉(静脉)采血、耳静脉采血、前肢头静脉采血、后肢小静脉采血等。二、 尿液的采集实验动物的尿液常用代谢笼采集,也可通过其他装置来采集。(一)、用代谢笼采集尿液代谢笼用于收集实
实验动物中常用的麻醉方法
(一)全身麻醉:麻醉药经呼吸道吸入或静脉、肌肉注射,产生中枢神经系统抑制,呈现神志消失,全身不感疼痛,肌肉松弛和反射抑制等现象,这种方法称全身麻醉。其特点为抑制深浅与药物在血液内的浓度有关,当麻醉药从体内排出或在体内代谢破坏后,动物逐渐清醒,不留后遗症。吸入麻醉法 麻醉药以蒸气或气体状态经呼吸道吸入
动物实验的接种途径和方法
动物实验的接种途径和方法是检验技师考试的内容,医学教育网搜集整理相关内容供大家参考。 动物实验的接种途径和方法包括: ①皮内接种:通常以背部皮肤为宜。 ②皮下接种:选用腹壁、背部或腹股沟等处。 ③肌肉接种:一般选用臀部和大腿部肌肉,若为禽类以胸部肌肉为宜。 ④静脉接种:家兔以耳静脉外缘为
动物所发现肺癌精准治疗新标记
发现基因及其编码蛋白质的异常是癌症精准治疗的基础。局部黏着斑激酶(focal adhesion kinase, FAK)是一种重要的非受体型酪氨酸激酶,在几乎所有的细胞中均有表达,可将细胞外的重要信号(如细胞生长、营养等)向细胞内传导,调控细胞的基本生物学功能。FAK在肺癌等肿瘤中表达增高并与病
脂质体介导的真核细胞转染实验——哺乳动物细胞选择标记
哺乳动物细胞的选择标记实验材料哺乳动物实验步骤一、腺苷脱氨酶(ADA) 1. 选择条件:培养液中加10 μg/ml 胸腺嘧啶脱氧核苷,15 μg/ml 次黄嘌呤,4 μmol/l 腺嘌呤-9-β-D-呋喃木糖苷(Xyl-A),及0.01~0.3 μmol/l 2‘-脱氧助间型霉索(dCF)。胎牛血
ULS标记实验
实验方法原理Universal Linkage System(ULS®;KREATECH Biotechnology BV)是用铂染色络合物与鸟嘌呤核苷的N7残基反应进行标记的方法。反应使核酸与铂荧光基团之间形成稳定的化学键。依据反应条件,ULS化合物在较低的程度上也与腺嘌呤形成络合物。该方法已用于
ULS标记实验
实验方法原理 Universal Linkage System(ULS®;KREATECH Biotechnology BV)是用铂染色络合物与鸟嘌呤核苷的N7残基反应进行标记的方法。反应使核酸与铂荧光基团之间形成稳定的化学键。依据反应条件,ULS化合物在较低的程度上也与腺嘌呤形成络合物。该
ULS标记实验
基本方案 实验方法原理Universal Linkage System(ULS®;KREATECH Biotechnology BV
抗体标记方法
Biotinylation of Antibody ( Contributed by Nanci Donacki) Antibody labeling (House Ear Institute)Labeling protocols using affinity markers. Coupling
动物实验与动物仪器
一、动物实验的主要目的 医疗器械的动物试验的主要目的是研究医疗器械的安全性,通常医学研究中的动物试验研究的主体可能是一种新诊治方法和原理,或一种新的药物的作用机理等等,它的主要研究目的是机理、有效性和安全性,这个研究可能与器械的使用存在联系,也可能不存在联系,且研究中可能没有涉及到植入或与
实验动物实验标本的采集实验——实验动物脑脊液采集
实验材料实验动物试剂、试剂盒消毒液仪器、耗材注射器实验步骤(1) 狗、兔脑脊液的采集:通常采取脊髓穿刺法,穿刺部位在两髂连线中点稍下方第七腰椎间隙。动物麻醉后侧卧位固定,头尾部尽量弯向腰部,去被毛。消毒后一手固定穿刺部位的皮肤,腰穿针垂直刺入,当有落空感及动物的后肢跳动时,针已达椎管内,抽去针芯,即
实验动物实验标本的采集实验——实验动物尿液采集
实验材料实验动物试剂、试剂盒水仪器、耗材收集器实验步骤尿液的采集 常用的采集方法较多,一般在实验前需给动物灌服一定量的水。(1) 代谢笼法:此法较常用,适用于大、小鼠。将动物放在特制的笼内。一般需收集 5 小时以上的尿液,最后取平均值。(2) 导尿法:常用于雄性兔、狗。动物轻度麻醉后,固定于手术台上
高地辛标记的DNA探针制备实验——基本方法
实验材料DNA试剂、试剂盒dTTPdUTPEDTASDS仪器、耗材水浴锅培养箱实验步骤1. 建立一个标准100 μl 反应体系,用10 μl,10×地高辛·11-dUTP/dTTP贮液,DNA酶Ⅰ酶量不变,15℃温育2 h。2. 取小份在微型胶中进行电泳以检测探针大小。3. 继续反应直到获得大
临床化学检查方法介绍动物实验介绍
动物实验介绍: 动物实验是在实验室内,为了获得有关生物学、医学等方面的新知识或解决具体问题而使用动物 进行的科学研究。动物实验必须由经过培训的、具备研究学位或专 业技术能力的人员进行或在其指导下进行。动物实验正常值: 无动物实验临床意义: 实验动物科学发展的最终目的,就是要通过对动物本身生命现
急性动物实验中常用的手术方法
急性动物实验中常以血压、呼吸等为指标,以静脉注射、放血等为实验方法。需要曝露气管、颈总动脉,颈外静脉,股动脉,股静脉,并做相应的插管,以及分离迷走神经,减压神经及股神经等。因此手术主要颈部及股部进行,现分述如下:(一)兔、狗颈部手术颈部手术的目的在于暴露气管、颈部血管并作相应的插管以及分离神经等。颈
病毒的培养方法实验——动物接种法
实验方法原理注意选择动物种类,年龄。按病毒侵袭部位的不同,选择适宜的接种途径,例如脑炎病毒以注射脑内最敏感。接种后经一定潜伏期,动物发病或死亡即进行解剖。根据动物的症状表现,器官病理改变,受染脏器组织悬液能在同种动物进行连续传代,并排除其他微生物污染的可能性等,即可证明有病毒的增殖。实验材料小白鼠实
急性毒性试验实验动物染毒方法

1.经口(胃肠道)接触目的是研究外来化合物能否经胃肠道吸收及求出经口接触的致死剂量(LD50)等。由于外来化合物可以污染饮水及食物,因此,此种染毒方式在卫生毒理学中占有重要地位。2. 灌胃是将液态受试化合物或固态、气态化合物溶于某种溶剂中,配制成一定浓度,装入注射器等定量容器,经过导管注入胃内。在每
实验动物给药和采血方法(一)
1.割(剪)尾采血当所需血量很少时采用本法。固定动物并露出鼠尾。将尾部毛剪去后消毒,然后浸在45℃左右的温水中数分钟,使尾部血管充盈。再将尾擦干,用锐器(刀或剪刀)割去尾尖0.3-0.5cm,让血液自由滴入盛器或用血红蛋白吸管吸取,采血结束,伤口消毒并压迫止血。也可在尾部作一横切口,割破尾动脉或静脉
常规动物实验模型制作(复制)方法(一)
一、肿瘤动物模型的建立将对数生长的肿瘤细胞收集 , 用无血清基质 10.0ml, 于 1500 转/ 分, 离心3min, 连续洗 3 次, 最后用无血清基质混匀, 用血球计数器计算肿瘤细胞数量( 平均 5 个中方格的细胞计数×104即是肿瘤数/ 毫升) 。 计算完肿瘤细胞总数, 再将 肿瘤细胞密度
动物的注射方法实验——腹腔注射法
实验材料小鼠试剂、试剂盒灭菌生理盐水仪器、耗材注射器(1 ml)7 号针头消毒煮沸器碘酒棉花75% 酒精棉花消毒干棉花实验步骤1. 注射器的准备与消毒(同「皮下注射法」)。2.腹腔注射2.1 抓取与固定方法同小鼠皮下注射实验。2.2 消毒下腹部皮肤,使鼠头部稍向下,以免针头刺入内脏(图 1,B)。2
常规动物实验模型制作(复制)方法(二)
四、呼吸系统疾病动物模型复制1、慢性支气管肺炎模型 常选用大鼠、豚鼠或猴吸入刺激性气体(如二氧化硫、氯、氨水、烟雾等)复制人类慢性气管炎。现发现猪粘膜下腺体与人类相似,且经常发生气管炎及肺炎,故认为是复制人类慢性气管炎较合适的动物。用去甲肾上腺素可以引起与人类相似的气管腺体肥大。2、肺气肿模型
常规动物实验模型制作(复制)方法(三)
六、Alzhermer病的动物模型SD大鼠200-250克。用3%戊巴比妥钠(35-40mg/kg体重)腹腔麻醉动物后,固定在脑立体定位仪上(参照大鼠全脑立体定位图谱),以前囟为零点,选出进刀坐标:前后坐标(AP)1.8mm,中线旁开(L)坐标1.0mm,腹侧坐标(v)4. 0mm。首先用牙科钻在上
实验动物给药和采血方法(二)
4.后肢胫部皮下静脉取血将兔仰卧固定于兔固定板上,或由一人将兔固定好。拔去胫部被毛,在胫部上端股部扎以橡皮管,则在胫部外侧浅表皮下,可清楚见到皮下静脉。用左手两指固定好静脉,右手取带有5(1/2)号针头的注射器内皮下静脉平行方向刺入血管,抽一下针栓,如血进入注射器,表示针头已刺入血管,即可取血。一次
动物组织研磨样品典型实验方法
TL系列动物组织研磨仪具有对称的一对高速大振幅的摇臂,通过研磨珠在样品管内来回不规则撞击及摩擦,在几秒到几分钟内轻松实现样品的研磨、粉碎、混合及细胞破壁。精细的研磨,最细可以达到5微米。对于不同的的样品,TL系列动物组织研磨仪需要用不同的条件来处理,这里面主要涉及研磨速度、研磨时间、研磨温度和研磨珠